使用脂质辅料的口服多肽传递系统
口服多肽传递系统的挑战
为了使口服多肽治疗有效,处方必须:
防止多肽在胃肠道中降解
促进多肽的渗透性
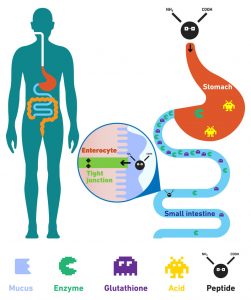
多肽需要被亲脂化后才能与脂质辅料结合
大多数多肽是亲水的,因此不能与脂质处方结合。他们需要被亲脂化(即增加LogP)。
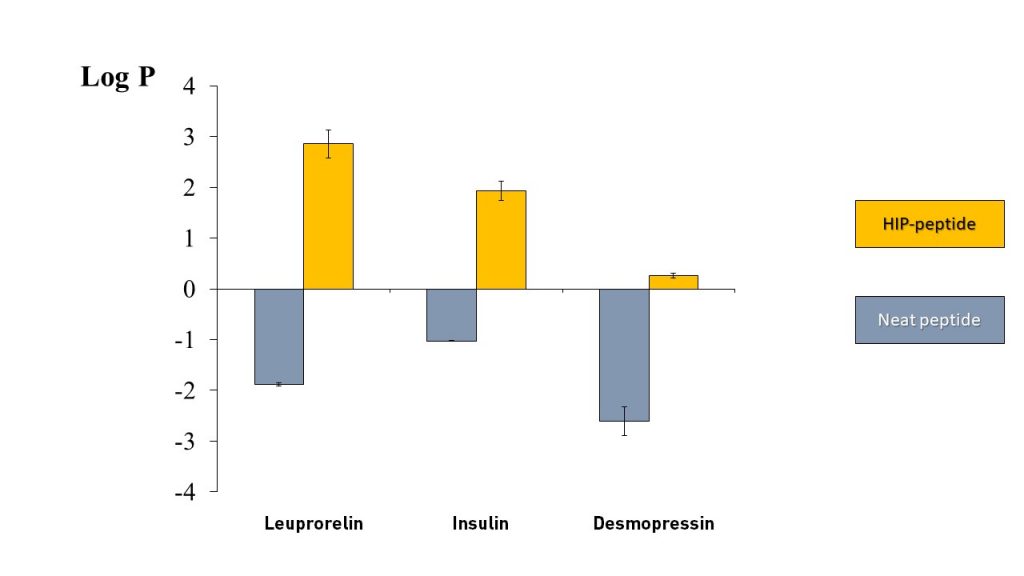
疏水离子对(HIP) 是一种增加多肽亲脂性的策略。以下三种模型的多肽用HIP亲脂化后,Log P显著增加,证实HIP-多肽是亲脂的。
自乳化给药系统(SEDDS):一种简单有效的解决方案
由油相、表面活性剂和溶剂的混合物组成,在整个消化过程中使药物保持溶解
对HIP-多肽提供有效的保护,免受酶降解和谷胱甘肽还原
透过肠粘膜细胞
实现对HIP-多肽的高载药量
固体脂质纳米粒(SLN)和纳米结构脂质载体(NLC):一种有潜力的解决方案
脂质纳米载体有望增加多肽向肠上皮细胞的传递,因为纳米级别微粒有利于细胞内转运。
固体脂质纳米粒(SLN)由室温和体温下的固态脂质组成,通常是长链脂肪酸甘油三酯或部分甘油酯、脂肪酸、蜡等。
纳米结构脂质载体(NLC)包含室温和体温下的固体和液体脂质。液体脂质作为固体脂质的结晶抑制剂。
纳米粒子在体外模型中被证明能够穿过粘液和肠上皮细胞。






